Calendario scientifico febbraio 2025
Diagnosi dell’emoglobinuria parossistica notturna (PNH)
Qual è il ruolo dell’immunofenotipizzazione nella diagnosi di PNH?
Misura principalmente il livello di emoglobina nel sangue durante episodi emolitici.
Identifica la presenza di anticorpi specifici che colpiscono le cellule ematiche nei pazienti con PNH.
Viene utilizzata per rilevare l’assenza di proteine legate a GPI (glicosilfosfatidilinositolo) sulla superficie delle cellule ematiche.
Congratulations!
That's the correct answer!
Sorry! That´s not completely correct!
Please try again
Sorry! That's not the correct answer!
Please try again
Notice
Please select at least one answer
CONTESTO SCIENTIFICO
Emoglobinuria parossistica notturna
L’emoglobinuria parossistica notturna (PNH) è un disturbo clonale delle cellule staminali ematopoietiche raro e potenzialmente letale, caratterizzato da emolisi intravascolare cronica causata dalla cascata complementare, trombosi e citopenie legate all’insufficienza midollare. Deriva da un’espansione mutazionale di un clone, che disattiva il gene PIG-A, situato sul cromosoma X, producendo una carenza di proteine legate a GPI (glicosilfosfatidilinositolo) sulla superficie di globuli rossi (RBC), monociti e granulociti. Queste includono due proteine regolatrici del complemento sulla membrana eritrocitaria, ovvero CD55 (fattore di accelerazione del decadimento – DAF) e CD59 (inibitore di membrana della lisi reattiva – MIRL). Una carenza di queste due proteine porta alla distruzione dei globuli rossi in vivo [1].
Diagnosi
La diagnosi di PNH prevede una serie di esami di laboratorio:
- Citometria a flusso degli antigeni legati a GPI che mostra le popolazioni di globuli rossi e bianchi negative
- Test di Coombs positivo
- Anemia con aumento della conta reticolocitaria
- Aumento della lattato deidrogenasi e della bilirubina
- Diminuzione dell’aptoglobina
- Emoglobina sierica libera ed emoglobinuria
- Danno d’organo associato da emolisi e/o trombosi [1].
La citometria a flusso è considerata lo standard aureo per la rilevazione dei cloni PNH e svolge pertanto un ruolo importante nella diagnosi, nel monitoraggio e nella gestione clinica dei pazienti con PNH. Il più recente aggiornamento delle linee guida di consenso ICCS/ESCCA [riassunto in 2] garantisce una rilevazione sensibile e accurata anche dei cloni PNH minori.
Il DryFlowEx PNH High-Sensitivity Assay Kit è stato sviluppato seguendo il più recente aggiornamento delle linee guida di consenso ICCS/ESCCA , che permette un elevato livello di sensibilità di rilevamento, in parte, grazie all’inclusione di FLAER (proaerolisina marcata con Alexa Fluor™ 488). FLAER si lega alle ancore GPI consentendo quindi di misurare la loro presenza o la loro assenza, indipendentemente da un particolare marcatore CD, su monociti e granulociti neutrofili.
Il kit fornisce due provette per paziente:
- Provetta RBC, contenente CD71, CD59 e CD235a
- Provetta WBC, contenente proaerolisina, CD157, CD45, CD64, CD24, CD14 e CD15
I cocktail per ogni provetta sono reagenti secchi, ovvero gli anticorpi vengono essiccati sulla superficie della provetta. Ciò consente un prolungamento della durata di conservazione e la conservazione e distribuzione a temperatura ambiente. I dettagli sulla preparazione dei campioni, sul gating e sull’interpretazione sono riportati nelle IFU.
CASO E RISULTATI
Una donna afroamericana di 19 anni si è presentata al pronto soccorso con tosse e urine scure; in precedenza era sana. L’anamnesi familiare mostrava che alla sorella era stato precedentemente diagnosticato il tratto falcemico.
Risultati ematologici
Un campione di sangue è stato inviato al laboratorio di ematologia, dove è stato eseguito un emocromo completo con un analizzatore della serie XN. I risultati (Fig. 1) mostravano che la paziente aveva un’anemia.
| Rerun | Order | Run | Test | Result | C | Unit |
| I | 2 | CBC Profile | ||||
| I | 2 | HGB | 90 | g/L | ||
| I | 2 | WBC | 2,56 | 10*9/L | ||
| I | 2 | PLT | 69 | & | 10*9/L | |
| I | 2 | RBC | 2,48 | 10*1… | ||
| I | 2 | HCT | 0,277 | L/L | ||
| I | 2 | MCV | 111,7 | fL | ||
| I | 2 | MCH | 36,3 | pg | ||
| I | 2 | MCHC | 325 | g/L | ||
| I | 2 | RDW-CV | 19,9 | % | ||
| RET Profile | ||||||
| R | 2 | RET# | 70,7 | 10*9/L | ||
| R | 2 | RET% | 2,9 | % | ||
| R | 2 | RET-He | 28,3 | pg | ||
| A | 2 | PLT-O | 69 | 10*3/… |
Fig. 1 Risultati del laboratorio di ematologia ottenuti con un analizzatore della serie XN
In sintesi, i parametri rilevanti per questo caso, con gli intervalli di riferimento interni all’ospedale indicati (tra parentesi), erano:
| 90 g/L | (115 – 155 g/L) |
| 2,48 x 1012/L | (3,9 – 5,6 x 1012/L) |
| 0,277 L/L | (0,36 – 0,48 L/L) |
| 2,9% | (0,5 – 1,5%) |
Risultati di altri test
Altri esami di laboratorio hanno confermato che l’anemia era di natura emolitica autoimmune:
| 3170 U/L | (87 – 225 U/L) |
| 1,9 mg/dL | (0 – 1,2 mg/dL) |
| 1,6 mg/dL | (0,2 – 0,7 mg/dL) |
|
Risultati dell’immunofenotipizzazione citometrica a flusso
La paziente è stata visitata da un ematologo, che ha inviato i campioni per i test per la PNH al laboratorio di citometria a flusso. È stata eseguita l’immunofenotipizzazione con il DryFlowEx PNH High-Sensitivity Assay Kit. L’analisi dei dati ha mostrato un significativo clone PNH in RBC e WBC, mostrando chiaramente l’assenza di antigeni legati a GPI.
I risultati relativi agli eritrociti, con la provetta RBC, hanno rivelato il 76,75% di cloni di tipo III e il 2,54% di cloni di tipo II (Fig. 2).

I risultati relativi ai globuli bianchi con la provetta WBC hanno mostrato un clone di granulociti neutrofili tra il 95 e il 97% (Fig 3) e un clone di monociti del 98% (Fig 4).
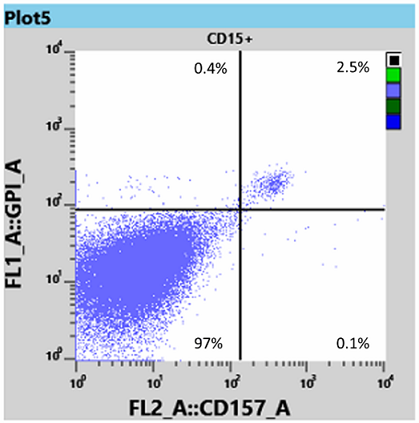
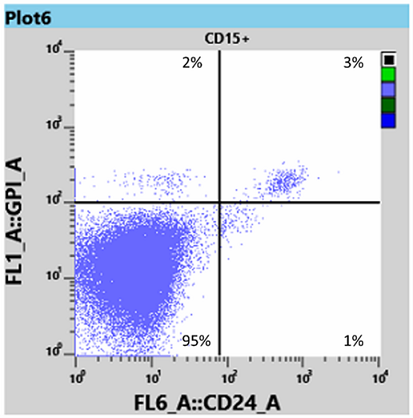
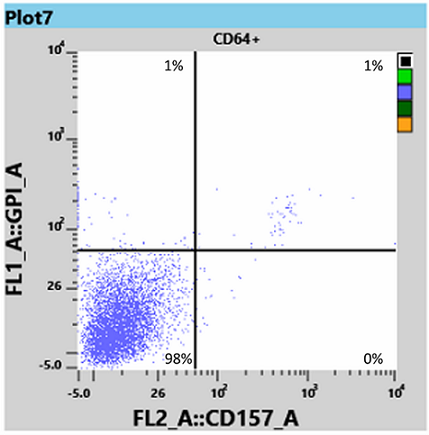
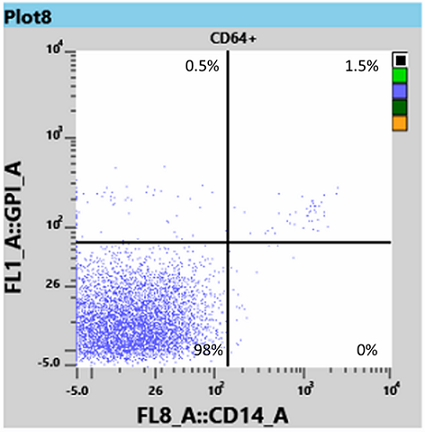
Da queste informazioni l’ematologo ha potuto determinare che la paziente aveva sia la forma omozigote (tipo III) che quella eterozigote (tipo II) della PNH e le ha somministrato Eculizumab, un’immunoterapia che si lega alla proteina C5 del complemento e inibisce l’attivazione del sistema complementare [3]. Questo legame impedisce la disgregazione dei globuli rossi nel flusso sanguigno.
Negli ultimi sei mesi l’emoglobina e la conta dei globuli rossi della paziente si sono stabilizzate nel range di normalità e non si sono verificati altri episodi emolitici.
RIFERIMENTI BIBLIOGRAFICI
[1] Cançado RD et al. (2021): Consensus statement for diagnosis and treatment of paroxysmal nocturnal haemoglobinuria. Hematol Transfus Cell Ther; 43(3):341-348. doi: 10.1016/j.htct.2020.06.006.
[2] Illingworth AJ, Marinov I, Sutherland DR (2019): Sensitive and accurate identification of PNH clones based on ICCS/ESCCA PNH Consensus Guidelines-A summary. Int J Lab Hematol; 41 Suppl 1:73–81. doi: 10.1111/ijlh.13011. PMID: 31069981.
[3] McKeage K (2011): Eculizumab. Drugs; 71:2327–2345. https://doi.org/10.2165/11208300-000000000-00000